자동유방 초음파의 임상적 적용
요약
자동유방 초음파는 기존 초음파(hand-held ultrasonography) 검사의 단점을 보완하기 위해 개발되었고 치밀유방 여성에서 유방암 검진 목적으로 주로 사용이 된다. 2021년 초음파 급여 확대 시행 항목에도 포함되었다. 자동유방 초음파는 영상 획득에서 유방 조직이 잘 포함되도록 촬영하는 것이 중요하며, 제대로 촬영된 영상과 재찰영이 필요한 영상에 대한 이해가 필요하다. 또한 자동유방 초음파에서만 구현이 되는 특징적인 디스플레이 방식과 양성, 악성을 구분하는 데 도움이 되는 소견들, 유방암 검진의 성능, 판독을 도와주는 컴퓨터보조진단(computer-aided detection/diagnosis, CAD) 시스템 적용까지 자동유방 초음파에 대한 전반적인 이해는 보다 현명하게 자동유방 초음파를 사용하는 데 필요하다. 이 종설에서는 기존 초음파와 다른 자동유방 초음파의 장점을 잘 살려 임상에서 적용할 수 있도록 자동유방 초음파의 촬영 방법, 영상의 질, 영상의 특징 및 판독에 이르는 포괄적인 지식을 전달하여 독자의 이해를 돕고자 한다.
중심 단어: 초음파; 유방종양; 판독; 암 조기 발견; 컴퓨터 보조 진단
Abstract
Automatic breast ultrasound (ABUS) has been developed to compensate for the shortcomings of hand-held ultrasound (HHUS) and is mainly used for breast cancer screening purposes in women with dense breasts. Since 2021, ABUS has been covered by the Korean National Health Insurance System. It is important to scan the entire breast on ABUS and to identify the poor-quality images requiring re-scanning. In addition, a general understanding of the unique ABUS display mode, distinguishing benign from malignant lesions, the diagnostic performance of breast cancer screening, and the application of computer-aided detection/diagnosis systems is necessary to use ABUS efficiently. This review explores the acquisition method, image quality, and image characteristics of ABUS to improve general understanding of this procedure and its advantages over HHUS, so that ABUS can be applied efficiently in clinical practice.
Keywords: Ultrasonography; Breast neoplasms; Early detection of cancer; Diagnosis, Computer-aided
서 론
자동유방 초음파는 치밀유방 여성의 유방암 검진을 위한 검사 장비로 승인이 되었다[ 1]. 기존 초음파(hand-held ultrasound) 검사는 유방 병변을 발견하고 평가하는 데 이견이 없는 우수한 검사이지만, 검사자에 의존적이고 재현성이 떨어지는 단점이 있다. 또한, 증가된 검진 수요를 채우기에는 의사 인력이 부족하여 검사자 한 명이 감당해야 할 업무량이 점점 증가되고 있는 실제적인 어려움도 있다. 기존 초음파 검사의 장점은 유지하며, 문제점을 극복하기 위해 개발된 자동유방 초음파는 병변의 방향과 기술 등을 조금 더 객관적으로 할 수 있고 재현성이 향상되어 추가 검사에도 유용하다. 촬영을 하는 방사선사의 교육에 긴 시간이 필요하지 않고 촬영 후 영상을 판독하는 의사에게도 시간 효율적인 방법이다[ 2- 4]. 자동유방 초음파의 주된 적응증은 치밀유방 여성의 유방 검진이다. 만져지는 멍울 등 진단적 상황에서 확립된 적응증은 없고, 절대적인 금기증도 없어 수술 후 유방 및 성형 후 유방에서도 사용이 가능하다[ 1]. 이 종설에서는 자동유방 초음파의 장점을 잘 살려 현명하게 임상에서 적용할 수 있도록 자동유방 초음파의 촬영 방법, 영상의 질, 영상의 특징 및 판독에 이르는 포괄적인 지식을 전달하고 이해를 돕고자 한다.
자동유방 초음파 영상 촬영 및 영상의 질
자동유방 초음파는 기존 초음파와 같이 누운 자세로 검사하며 한쪽 유방에서 전후방, 내측 및 외측 방향으로 세 번 검사를 한다. 유방이 작을 경우에는 두 번 검사를, 큰 경우에는 위나 또는 아래 방향으로 추가 검사를 시행한다( Fig. 1). 기존 초음파에 포함되는 액와부가 자동유방 초음파에서는 포함되지 않으며 이는 자동유방 초음파의 제한점이다. 양측 유방의 검사는 약 15분이 소요된다. 자동유방 초음파 영상은 기존 초음파와 같이 축상면(axial, transverse)으로 얻게 되며 워크스테이션으로 데이터 전송 후 시상면(sagittal) 및 관상면(coronal) 영상으로 삼차원 재구성이 이루어진다. 슬라이스 두께와 유방 크기에 따라 다르지만 보통 약 2,000개의 이미지가 생성된다[ 5]. 판독 모드를 선택할 수 있으며( Fig. 2), 커서를 영상면에서 보이는 종괴 및 병변에 놓으면 다른 영상면에서 해당 병변이 자동적으로 보인다. 이상 유무 및 영상 수에 따라 다르지만, 평균 판독 시간은 9분이다[ 6]. 모든 유방 조직은 빠지는 부분 없이 충분히 포함되어 촬영되어야 한다. 탐촉자와 피부 사이의 접촉을 최대화하기 위해 자동 유방 초음파 전용 로션을 사용하며 접촉이 안 된 부위에서는 인공물이 형성되어 유방 병변 평가가 어려울 수 있다. 숙련된 조작으로 탐촉자가 포함된 스캔상자(scanning box)를 유방에 놓고 부드럽지만 충분하게 유방을 압박해야 한다( Figs. 3 and 4). 스캔이 완료되면 획득된 유방의 관상면 피부 영상이 모니터에 표시되며, 이를 통해 전체적인 윤곽 및 적절한 접촉 유무 및 피부 주름 등 획득된 영상의 적절성을 간략하게 평가한다. 적절하지 않는 경우 부족한 부분을 다시 촬영하여 재촬영을 위해 환자가 다시 내원하는 번거로움을 줄일 수 있다. 전후방 기본 영상에서는 유두가 영상의 중앙에 위치해야 하며, 내측 및 외측 영상에서는 유두가 영상의 가장자리에 위치하여 포함하고자 하는 유방이 충분히 포함되도록 해야 한다. 유방이 큰 경우에는 추가로 영상을 획득해야 하고 깊이 있는 유방 조직이 잘 포함되었는지 확인하여 필요 시 스캔 깊이를 조정해야 한다. 스캔 깊이는 브래지어 컵 사이즈에 따라 선택할 수 있다( Fig. 5).
영상 디스플레이 모드와 관상면 영상
영상 획득이 완료되면, 자동유방 초음파 전용 워크스테이션을 통해 축상, 시상 및 관상 영상면으로 영상을 검토한다. 관상면은 자동유방 초음파의 독특한 영상면이며, 유방 전체의 윤곽 및 해부학적 구조를 보다 쉽고 포괄적으로 보여준다는 장점이 있다. 대부분의 유방암 검진 연구에서는 관상면만을 선택하여 판독을 했으며, 전체 영상을 보지 않기 때문에 검토 및 판독에 드는 시간이 단축되는 장점이 있음을 강조했다. 하지만, Chae 등[ 7]의 연구에 의하면 456개의 잠재적 병변의 발견율이 축상면에서 80%로 관상면의 67%보다 높았다. 악성 병변 및 양성 병변 모두 관상면보다 축상면에서 통계적으로 의미 있게 더 많이 발견되었다. 축상면은 기존 유방 초음파 영상과 같기 때문에 검사자에게 더 익숙한 영상면이며, 병변을 놓치지 않기 위해서는 축상면, 관상면 모두를 함께 검토하는 것이 바람직하다. 관상면에서 특징적으로 보이며, 병변 평가에 유용한 소견들이 있다. 뒷당김 현상(retraction phenomenon)은 병변 주위로 별모양 형태가 특징적이며, 악성종양을 시사한다( Fig. 6) [ 8]. 뒷당김 현상의 악성을 진단하는 민감도는 80-89%, 특이도는 96-100%로 알려져 있고, 관상면에서 이 현상이 가장 잘 보인다[ 5, 8, 9]. 그러나 빠르게 자라는 유방암에서는 나타나지 않을 수도 있다[ 8]. 흰벽징후(white-wall sign)는 무에코성 병변을 따라 에코가 높은 테두리가 보이는 것으로 관상면에서 잘 나타나며, 기존 유방 초음파에서 보였던 병변의 후방음향 증가(posterior acoustic enhancement)에 해당한다( Fig. 7). 흰벽징후는 낭종, 섬유선종, 유두종 등 양성 병변에서 주로 관찰되나, 드물게 악성에서도 보일 수 있다[ 5, 9, 10]. 자동유방 초음파의 영상 영역(field of view)이 기존 초음파보다 넓기 때문에 관상면에서 늘어난 유관, 유관내 병변 등 비종괴양 병변을 발견하고 평가하는 데 유용하다. 관내상피암과 유두종양은 흔하게 비종괴양 병변으로 보이며, 자동유방 초음파의 관상면은 기존 초음파에 비해 병변의 범위를 보다 정확하게 평가할 수 있다( Fig. 8) [ 5, 8, 9].
유방암 검진과 자동유방 초음파
유방촬영술 검진은 유방암 사망률을 감소시키는 것으로 증명된 유일한 검진 방법이지만, 치밀유방에서는 유방촬영술의 민감도가 현저히 감소한다. 또한 치밀유방은 유방암 발생의 중등도 위험인자로도 알려져 있다[ 11]. 우리나라에서는 20여 년 전부터 유방암 발생률이 지속적으로 증가하였으며, 2020년에는 약 25,000명에서 유방암이 새롭게 진단되었고, 한국 여성에서 가장 흔하게 발생하는 암이 되었다. 나이가 들면서 유방암 발생률이 계속 증가하는 서양과는 달리, 한국에서는 나이가 증가하면서 유방암 발생이 증가하다가 45-49세에 가장 많이 발생하고, 그 이후 감소하는 것이 서양과 구별되는 한국 유방암의 역학적 특징이다[ 12, 13]. 또한, 서양 여성과 비교할 때 한국을 포함한 동양 여성에서 치밀유방의 빈도가 높으며, 유방암이 가장 많이 발생하는 한국 40대 여성에서의 치밀유방 빈도는 77-85%나 된다[ 14]. Park 등[ 15]은 한국 여성에서도 치밀유방은 유방암 발생의 위험인자이며, 치밀유방을 갖는 한국 여성은 주로 지방으로 구성된 유방을 갖는 여성에 비해 유방암의 발생률이 3.8-5배 높다고 보고했다. 유방 초음파 검진을 통한 사망률 감소에 대한 증거가 불충분하기 때문에, 대부분의 검진 가이드라인은 유방 초음파를 권고하지 않지만, 미국방사선의학회에서는 치밀유방 여성에서 유방 초음파 검사를 추가할 것을 권고하고 있다[ 16]. 개정된 한국 유방암 검진 가이드라인은 유방 초음파 검진을 권고하지도 반대하지도 않는다[ 17]. 장기적인 추적 검사 결과 등의 자료가 충분하지는 않지만, 추가적인 유방 초음파 검진은 유방암, 특히 조기 유방암 발견에 높은 민감도를 보였고, 간격암의 낮은 발생 빈도를 보였다[ 18- 20]. 40대 일본 여성을 대상으로 유방촬영술 단독 검진과 유방촬영술, 초음파 병용 검진의 진단능을 분석한 전향적 무작위 시험(Japan Strategic Anti-cancer Randomized Trial)에서 병용 검진은 1,000명당 1.84개의 유방암을 추가로 발견했다[ 18]. 자동유방 초음파 검진의 유방암 발견 능력은 기존의 유방 초음파와 비슷했다. 미국 13개 기관에서 유방촬영술에서 치밀유방을 보인 여성 15,318명을 대상으로 전향적인 자동유방 초음파 검진을 시행했고 1,000명당 1.9개의 유방암을 추가로 발견했다. 또한 자동유방 초음파에서만 보였던 유방암의 93%는 침윤성 유방암이었다[ 21]. 한국 40대 무증상 여성 959명을 대상으로 유방촬영술 없이 자동유방 초음파 단독 검진을 시행한 다기관 전향적 연구에 의하면, 1,000명당 유방암 발견율은 5.2명, 소환율 9.8%, 민감도 83%, 특이도 90%였다[ 22]. 일본 40대 여성을 대상으로 한 유방 초음파 병용 검진의 유방암 발견율 및 진단능과 비슷했다[ 18]. 자동유방 초음파 검진 또한 기존 초음파와 같이 높은 소환율, 조직 검사율, 낮은 양성 예측도를 보이는 문제점이 있다. 위양성 결과를 줄이기 위해 노력해야 한다. 자동유방 초음파에서 이상 소견이 보일 경우 자동유방 초음파 유도하 조직 검사가 불가능하기 때문에 기존의 초음파(hand-held ultrasound)를 한 번 더해야 하는 것 또한 문제점이다.
자동유방 초음파와 컴퓨터보조진단
인공지능과 딥러닝 등 컴퓨터 기술의 비약적 발전으로 computeraided detection/diagnosis (CAD) 시스템은 병변을 발견하고 진단하는 데 여러 영역에서 도움을 주고 있으며 기존 초음파뿐 아니라 자동유방 초음파에서도 적용이 가능하다. CAD 시스템은 의사의 진단능을 향상시키고 영상 판독 시간을 단축시켜주는 장점이 있다. 특히 자동유방 초음파 판독의 경험이 의사들에서 판독능을 의미 있게 향상시켰다는 연구 결과도 있었다[ 23]. 저자는 QVCAD 시스템(Qview Medical Inc., Los Altos, CA, USA)을 이용했고 이 시스템은 병변의 경계면, 에코 양상, 후방 음영, 구조 왜곡 등 악성을 시사하는 특징을 자동적으로 추출하고 종합하여 악성이 의심되는 5 mm 이상의 병변에 자동적으로 악성이 의심됨을 표시해 준다( Figs. 9 and 10) [ 5].
결 론
자동유방 초음파는 재현성이 우수하고, 객관적으로 병변의 발견 및 평가, 기술하는 데 유용하고 판독하는 의사에게 시간적으로 효율적인 검사 방법이다. 치밀유방 여성에서 추가적으로 시행되는 유방암 검진이 주된 적응증이다. 기존 초음파와 다른 자동유방 초음파의 특징과 장단점을 잘 이해하여 임상에서 적용하는 것이 중요하다.
Figure 1.
Acquisition view of automated breast ultrasound. Anteroposterior (AP), medial and lateral view are basic acquisition views. Superior and inferior views are also obtained in the case of large breast size. 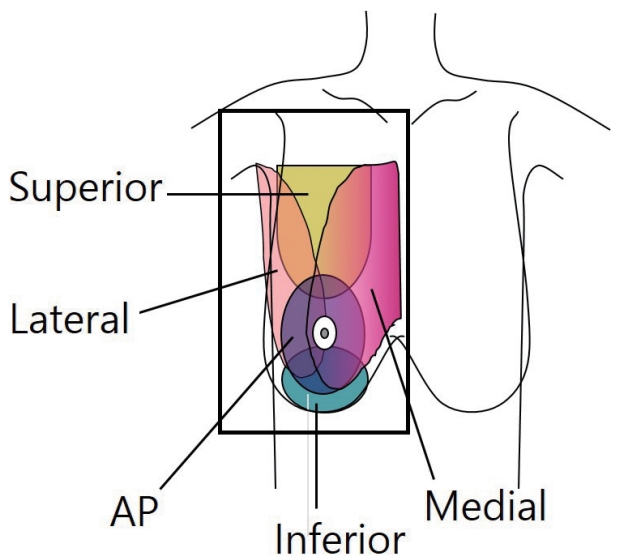
Figure 2.
Display mode of automated breast ultrasound. Axial dominant mode and coronal dominant mode, which can provide a view of all three image planes, are widely used. For breast screening, the coronal stack mode is sometimes preferred. 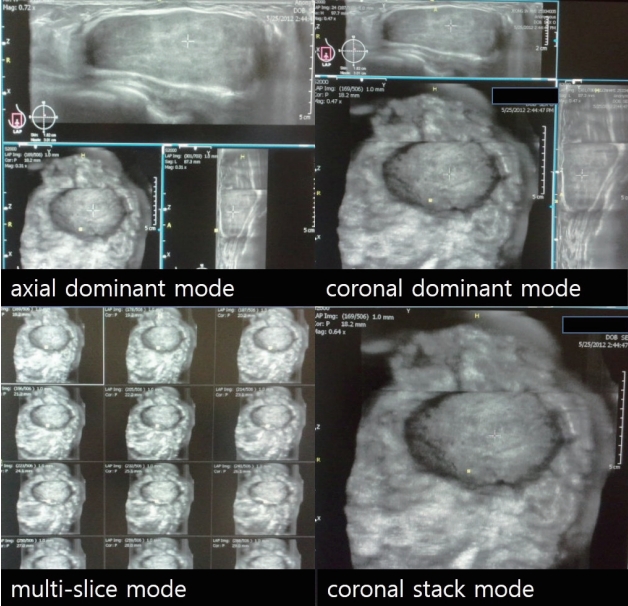
Figure 3.
Representative example of a high-quality image. The nipples (yellow squares) are properly positioned and all breast is included at the skin layer. AP = anteroposterior. 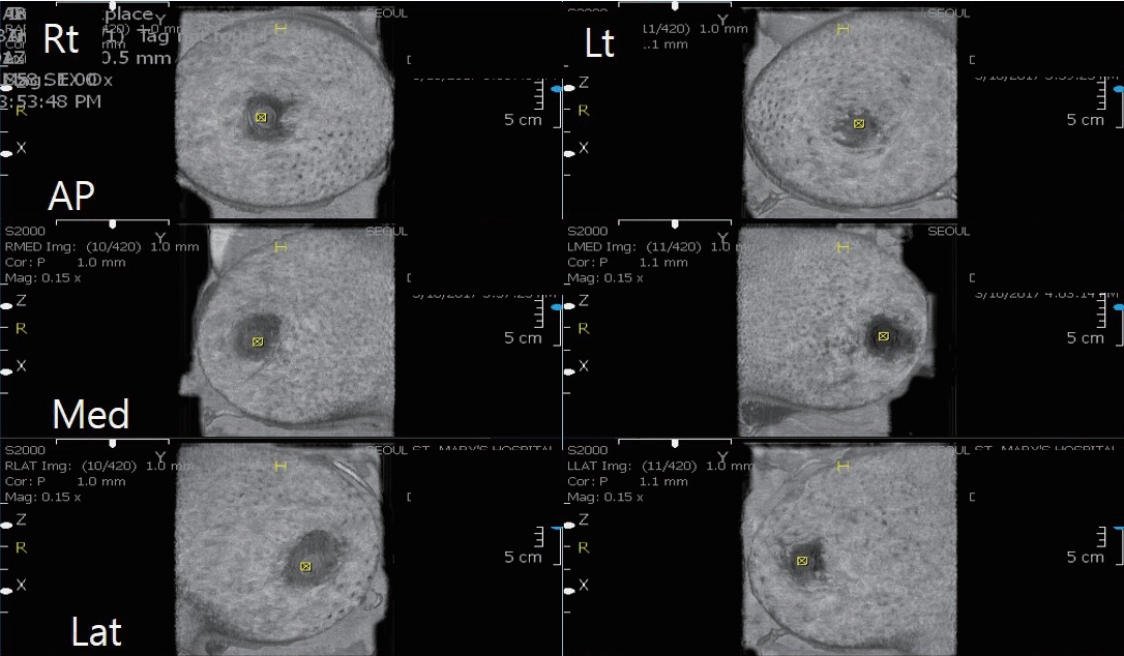
Figure 4.
Representative example of a poor-quality image. The right lower breast and left upper and mid breast are not completely included (circles). AP = anteroposterior. 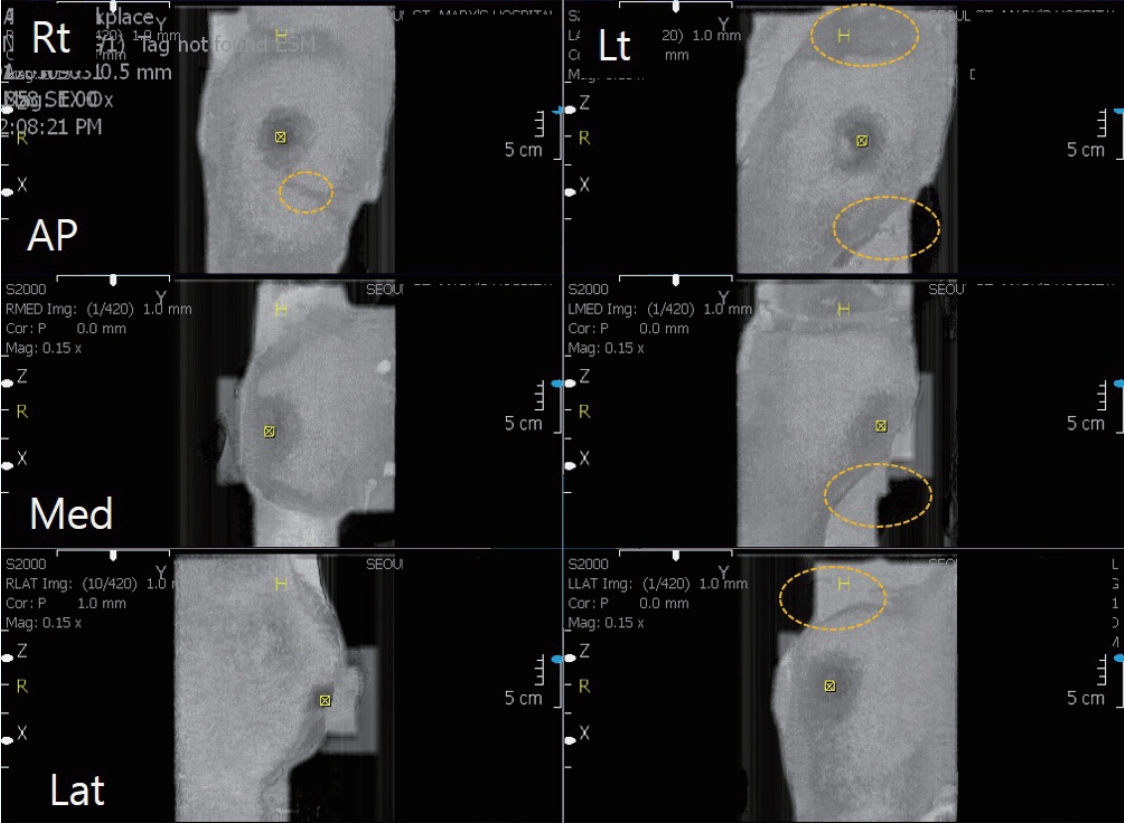
Figure 5.
Representative example of additional views. (A) Breast parenchyma is still noted in the far upper portion on left anteroposterior (AP) view due to large breast size. (B) Superior view is obtained such that the nipple (yellow square) is positioned below and the upper breasts are included. (C) Deep parenchyma is not completely included on right AP view. (D) The scan depth is expanded from 4.5 cm to 5.5 cm. The rescanned image includes all breast tissue and pectoralis muscle. 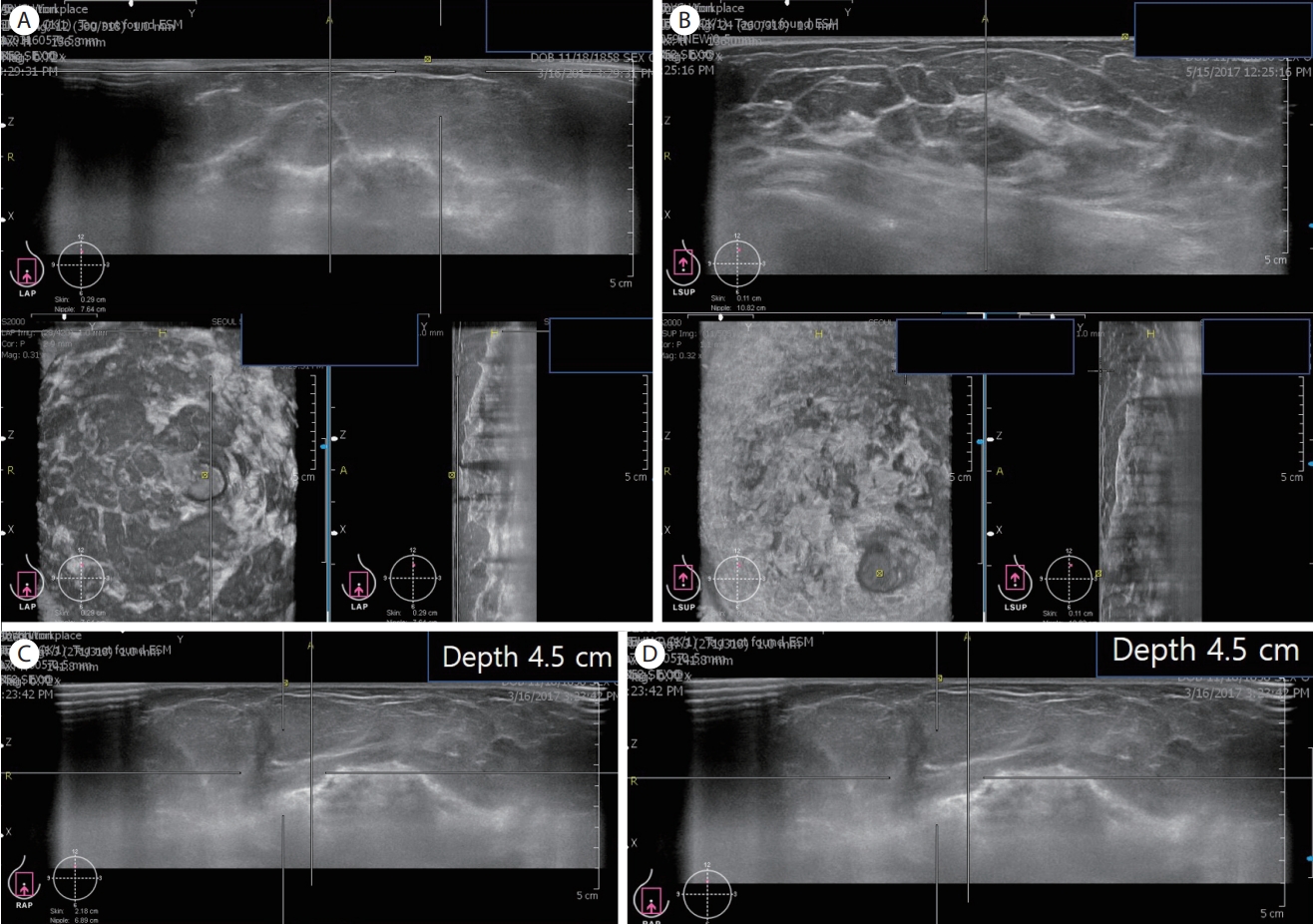
Figure 6.
Retraction phenomenon. Irregular spiculated hypoechoic mass showing the retraction phenomenon is well demonstrated on coronal view. Invasive breast cancer is confirmed. 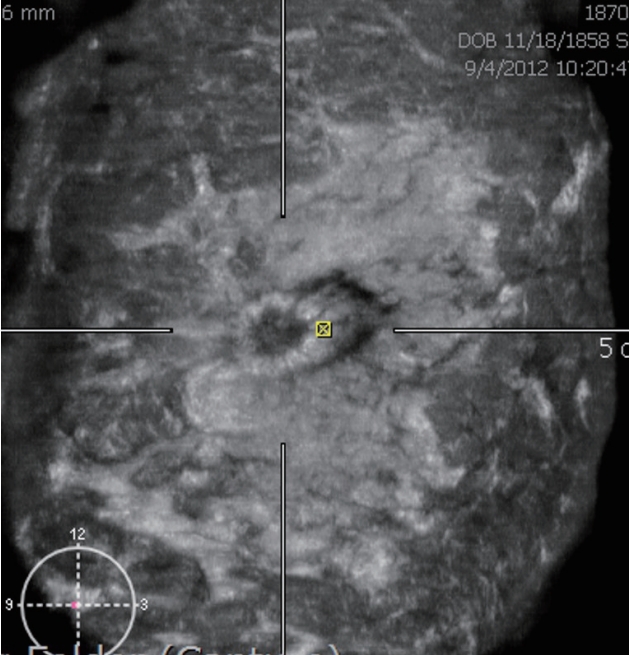
Figure 7.
White-wall sign. Echogenic wall around the anechoic cyst is shown on coronal view. 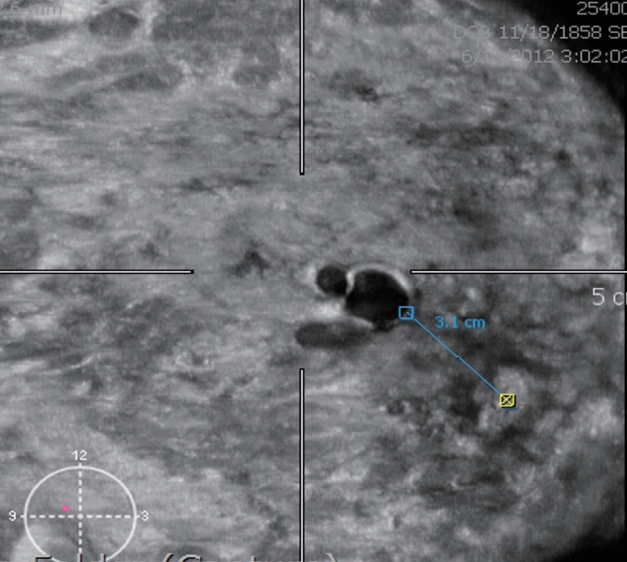
Figure 8.
Non-mass lesion. Coronal view shows a segmental nonmass lesion (arrowheads), which appears as tubular ductal change (arrowheads) on the transverse view. An atypical papillary tumor is confirmed. 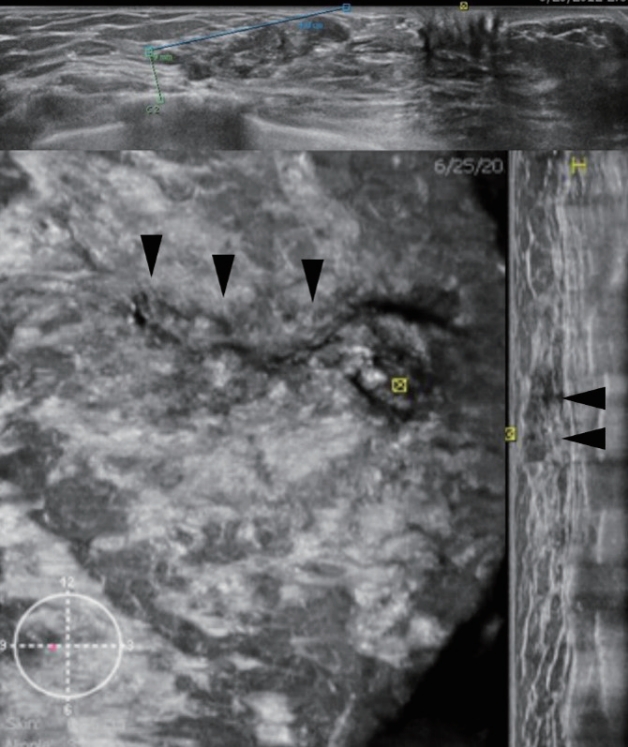
Figure 9.
True-positive case. Computer-aided detection/diagnosis detect a suspicious irregular hypoechoic mass and mark it as a green circle. Invasive breast cancer is confirmed. 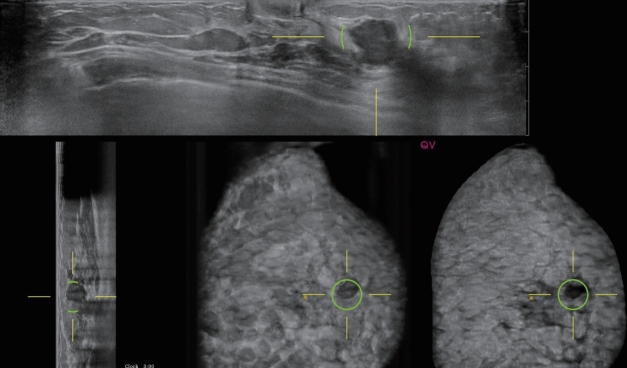
Figure 10.
False-negative and -positive cases. (A) Computer-aided detection/diagnosis does not detect a suspicious irregular hypoechoic mass. Invasive breast cancer is confirmed. (B) Computer-aided detection/diagnosis erroneously detect a rib as a suspicious mass and mark it as a green circle. 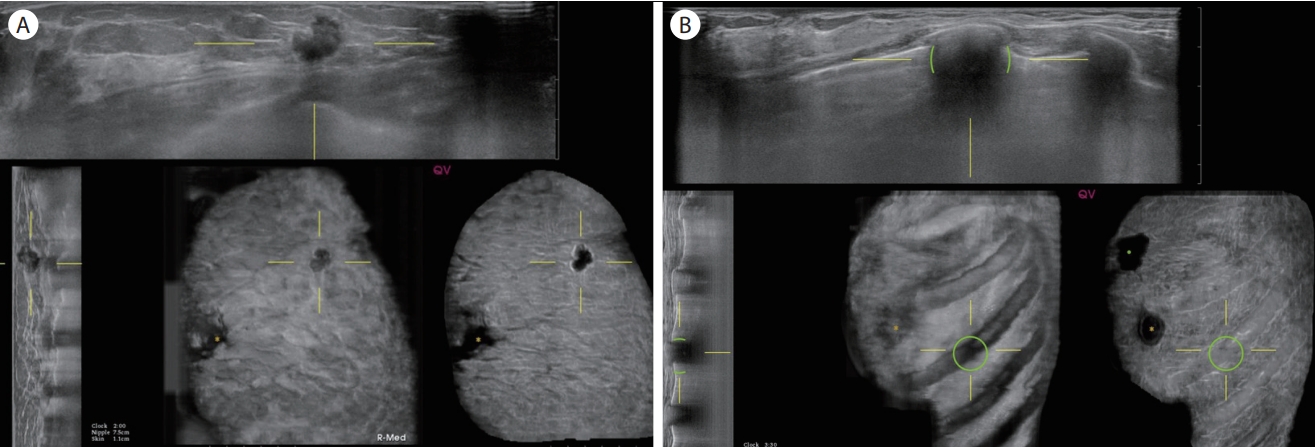
REFERENCES
1. Kaplan SS. Automated whole breast ultrasound. Radiol Clin North Am 2014;52:539–546.   4. Kelly KM, Dean J, Comulada WS, Lee SJ. Breast cancer detection using automated whole breast ultrasound and mammography in radiographically dense breasts. Eur Radiol 2010;20:734–742.   5. Kim SH, Kim HH, Moon WK. Automated breast ultrasound screening for dense breasts. Korean J Radiol 2020;21:15–24.   6. Skaane P, Gullien R, Eben EB, Sandhaug M, Schulz-Wendtland R, Stoeblen F. Interpretation of automated breast ultrasound (ABUS) with and without knowledge of mammography: a reader performance study. Acta Radiol 2015;56:404–412.   7. Chae EY, Cha JH, Kim HH, Shin HJ. Comparison of lesion detection in the transverse and coronal views on automated breast sonography. J Ultrasound Med 2015;34:125–135.   8. van Zelst JCM, Mann RM. Automated three-dimensional breast US for screening: technique, artifacts, and lesion characterization. Radiographics 2018;38:663–683.   9. Rella R, Belli P, Giuliani M, et al. Automated breast ultrasonography (ABUS) in the screening and diagnostic setting: indications and practical use. Acad Radiol 2018;25:1457–1470.   10. Vourtsis A, Kachulis A. The performance of 3D ABUS versus HHUS in the visualisation and BI-RADS characterisation of breast lesions in a large cohort of 1,886 women. Eur Radiol 2018;28:592–601.   11. Freer PE. Mammographic breast density: impact on breast cancer risk and implications for screening. Radiographics 2015;35:302–315.   15. Park B, Cho HM, Lee EH, et al. Does breast density measured through population-based screening independently increase breast cancer risk in Asian females? Clin Epidemiol 2018;10:61–70.   16. Mainiero MB, Moy L, Baron P, et al. ACR appropriateness criteria(R) breast cancer screening. J Am Coll Radiol 2017;14:S383–S390.  17. Lee EH, Park B, Kim NS, et al. The Korean guideline for breast cancer screening. J Korean Med Assoc 2015;58:408–419.  18. Ohuchi N, Suzuki A, Sobue T, et al. Sensitivity and specificity of mammography and adjunctive ultrasonography to screen for breast cancer in the Japan Strategic Anti-cancer Randomized Trial (J-START): a randomised controlled trial. Lancet 2016;387:341–348.   19. Brem RF, Lenihan MJ, Lieberman J, Torrente J. Screening breast ultrasound: past, present, and future. AJR Am J Roentgenol 2015;204:234–240.   21. Brem RF, Tabár L, Duffy SW, et al. Assessing improvement in detection of breast cancer with three-dimensional automated breast US in women with dense breast tissue: the SomoInsight Study. Radiology 2015;274:663–673.   22. Choi WJ, Kim SH, Shin HJ, et al. Automated breast US as the primary screening test for breast cancer among East Asian women aged 40-49 years: a multicenter prospective study. Eur Radiol 2021;31:7771–7782.   23. Xu X, Bao L, Tan Y, Zhu L, Kong F, Wang W. 1000-case reader study of radiologists’ performance in interpretation of automated breast volume scanner images with a computer-aided detection system. Ultrasound Med Biol 2018;44:1694–1702.  
|
|





















