간내 낭성 병변의 초음파 진단
Diagnosis of Cystic Hepatic Lesions on Ultrasonography
Article information
Trans Abstract
Cystic hepatic lesions are fluid-filled spaces within the liver, and are frequently encountered in clinical settings on a spectrum from benign to malignant disease. Ultrasonography has a critical role in primary evaluation, characterization, and monitoring of these lesions. This review comprehensively outlines the ultrasonographic findings associated with cystic hepatic lesions, including their classification, imaging features, diagnostic complexities, and clinical implications.
서 론
간내 낭성 병변은 간 내에 다양한 형태의 낭종 또는 낭종 모양의 병변을 의미한다. 이러한 낭성 병변은 간 내 조직 내에서 액체가 축적되어 형성되며 다양한 원인과 형태를 가질 수 있다. 간내 낭성 병변의 유병률은 지역에 따라 다양한 유병률이 보고되고 있으며 양성 간 낭종의 경우 미국에서 약 15–18% 정도로 보고되고 있다[1]. 또한, 국내의 한 후향적 연구에서 단일 기관에 방문한 양성 간 병변 환자 중 33.7%가 간내 낭성 병변을 보여 간내 혈관종(52.2%) 다음으로 가장 흔한 양성 간 병변이 다[2]. 간내 낭성 병변은 대부분 무증상으로 우연히 발견되지만, 단순 간낭종이라 하더라도 병변의 위치 및 크기에 따라 복부 불편감, 소화 장애 및 통증과 같은 증상이 동반될 수 있고 이 경우 치료가 필요한 낭종 내 출혈이나 감염 또는 파열과 같은 합병증 여부를 배제할 수 없다. 또한, 다방성의 중격을 가지거나 두꺼운 낭벽을 보이는 일부 간내 낭성 종양의 경우에는 악성 종양으로 진행할 가능성이 있어 수술적 절제가 원칙이 되기도 하므로, 낭성 병변의 영상학적 특징을 명확히 알고 추적 또는 치료 계획을 설정하는 것이 매우 중요하다. 상복부 초음파 검사는 안전하고 비침습적으로 이러한 영상학적 특징을 쉽게 확인할 수 있는 검사로, 낭성 병변의 크기, 개수, 모양 및 위치를 확인하고 낭종 벽의 두께, 내부 구조나 에코 특성 등을 확인하여 낭성 병변의 임상적 위험도를 예측할 수 있다. 또한 도플러 초음파를 이용하여 병변 내 혈류의 여부 및 시술 시 병변과 혈관과의 관계를 시각화하여 도움을 받을 수 있고, 병변의 크기와 내부 상태를 정기적으로 확인하며 추적 관찰하는 데에도 초음파 검사가 유용하게 사용될 수 있다. 따라서, 본고에서는 임상 환경에서 마주칠 수 있는 간내 낭성 병변을 소개하고 그 임상적 의의와 복부 초음파 상의 특징을 정리하였다.
본 론
단순 간 낭종(Simple hepatic cyst)
단순 간 낭종은 간 실질 내에 얇은 막으로 이루어진 공간이 생겨 그 속에 액체가 들어 있는 병변이다. 주변막을 이루고 있는 조직은 매우 얇은 정상 조직이며, 내부에 고여 있는 것도 정상 체액이다. 초음파 검사에서 둥근 형태로 보이며 낭종 내부의 액체로 인해 초음파 신호가 완전히 투과하고 반사되지 않아 무에코 병변으로 보인다(Fig. 1A). 벽은 얇고 미세하여 초음파로는 잘 감별되지 않으며 일반적으로 내부 액체와 구분되어 특별한 이상 소견이 없으면 매끈하게 보인다. 초음파 신호가 낭종 내부의 액체를 투과하고 액체 뒷면에 있는 구조물에서 초음파가 반사되기 때문에 초음파 상 후방 음영이 관찰되는게 특징이다. 초음파를 통해 단순 간 낭종의 크기를 측정하고 위치를 정확하게 확인할 수 있어 배액과 같은 시술에 도움을 받을 수 있으며 낭종이 성장하거나 변화하는지 추적하는데도 초음파가 유용하게 사용된다. 단순 간 낭종에 이차적으로 출혈이나 감염이 발생하는 경우를 복잡 간 낭종(complicated hepatic cyst)이라고 한다. 낭종에 출혈이 발생하면 내부가 비균질적인 고에코로 보일 수 있으며 응고된 혈액으로 인해 불규칙적인 유두상의 고형물질이 보이기도 하며 초음파 검사 시 통증이 발생할 수도 있다(Fig. 1B). 낭종에 감염이 발생하면 내부가 고에코로 보일 수 있으며 낭종 벽이 두꺼워질 수 있다(Fig. 1C). 증상을 동반하는 큰 복잡 간 낭종은 배액 및 경화술과 같은 내과적 치료 혹은 복강경을 이용한 개창술이나 낭종 절제와 같은 수술적 치료가 필요할 수 있다. 다만 초음파 상으로 복잡 간 낭종과 전암성 혹은 암성 간 낭종과 구분이 어려울 수 있어서 computed tomography (CT)나 magnetic resonance imaging (MRI)와 같은 영상검사를 통해 감별진단해야 한다. 한편 단순 간낭종은 대부분 무증상으로 치료가 필요하지 않지만 증상이 있는 경우에는 복잡 간 낭종과 같이 내과적 혹은 수술적 치료를 고려할 수 있다. 만약 수술적으로 제거한 경우 조직검사 상 악성의 증거가 있다면 반드시 낭종 전체를 절제해야 한다.

Simple hepatic cyst. (A) A cyst exhibiting well-defined, anechoic characteristics with no septation. Lateral shadowing and posterior enhancement can be seen (arrows). (B) A small cyst with internal echogenic material (arrow). (C) A large cyst with internal sludge-like material in the dependent portion (arrow).
다낭성 간 질환(Polycystic liver disease)
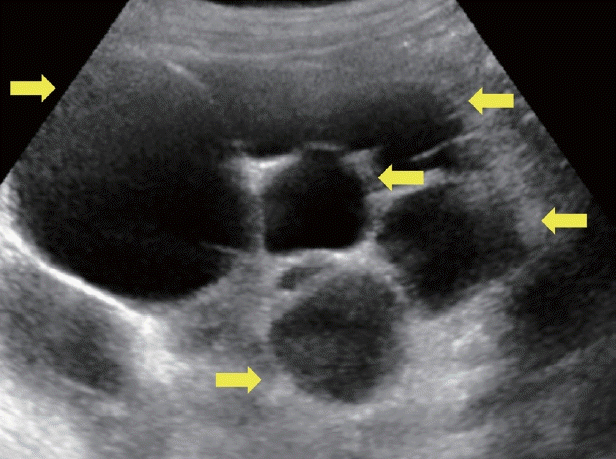
다낭성 간 질환은 간 내에 10개를 초과하는 낭종이 동시에 나타나는 질환을 말한다[3]. 다낭성 간 질환은 80–90%에서 다낭성 신장 질환과 동반되어 나타나며 단독으로 다낭성 간질환만 나타나는 경우의 유병률은 1–10:1,000,000 정도로 알려져 있다[4]. 초음파 상 낭종들의 크기는 다양하며 위치는 간 내 어디에든 발생할 수 있으며 내부의 중격, 혈류, 혈액 등에 따라 다양한 에코 패턴을 나타낼 수 있다(Fig. 2). 낭종 벽 두께는 종류에 따라 다를 수 있고 단순 간 낭종과 마찬가지로 낭종 뒷면에 후방 음영이 나타날 수 있다. 일부 낭종은 초음파 도플러를 통해 혈류를 확인할 수 있다. 낭종 벽이 두꺼워지거나 내부의 고에코 음영이 보이는 경우 낭성 감염을 의심할 수 있다. 단순 간 낭종과 마찬가지로 증상이 없는 경우 치료는 필요하지 않다. 하지만 복통, 위장관 역류, 호흡곤란과 같은 증상이 있거나 낭성 감염 및 파열 등의 증상이 있는 경우 낭종의 형태에 따라 소마토스타틴 유사체와 같은 약물 치료, 배액술, 수술적 치료 등을 고려할 수 있다[4].
간내 낭성 종양(Hepatic cystic tumor)
간내 낭성 종양은 간 내에서 발생하는 낭성 형태의 종양으로 다양한 종류와 형태를 가질 수 있다. 대부분의 간내 낭성 종양은 양성으로 특별한 치료 없이 관찰해도 되나 일부는 악성일 수 있다. 초음파만으로는 감별이 어렵기 때문에 추가로 CT, MRI, magnetic resonance cholangiopancreatography (MRCP), endoscopic retrograde cholangiopancreatography 등의 검사를 통해 진단에 도움을 얻어야 한다.
점액성 낭성종양(mucinous cystic neoplasm)
점액성 낭종종양은 이전에 담관낭선종(biliary cystadenoma)과 담관낭선암(biliary cystadenocarcinoma)으로 알려진 질환으로 전체 간내 낭성 병변의 3–5%를 차지한다[5]. 담관 점막층을 이루는 입방세포(cuboidal cell) 혹은 원주세포(columnar cell)를 상피세포로 하는 다방성 낭이 간실질에 만들어지는 것으로 점액을 분비하여 낭 내용물을 형성하며 대부분 무증상이나 낭성 종양 자체나 분비된 점액에 의해 담관폐쇄나 간피막 혹은 주변 장기의 압박이 일어나면 증상을 일으킨다. 초음파에서 간 내에 낭벽과 중격을 가진 크기가 큰(1.5–35 cm) 단일 낭성병변이 있으면 의심할 수 있다(Fig. 3) [6,7]. 무에코성 낭성병변 내부에 유두상 돌기나 중격이 관찰되며 중격에는 석회화가 보일 수도 있으며 조영증강 초음파 검사에서 내부 중격의 조영증강을 확인할 수도 있다. 담관낭선암으로 진행하면 낭벽이나 중격이 두꺼워지나 영상 검사만으로 담관낭선종과 담관낭선암을 구별하기는 어렵다. 따라서 점액성 낭성종양을 발견하면 수술적 치료가 원칙이다.

Mucinous cystic neoplasm. (A) An irregularly-margined, lobulated, septated cyst with posterior enhancement (arrow). (B) Axial T2-weighted magnetic resonance imaging of a lobulated hyperintense cystic lesion with hypointense septa (arrow). (C) Axial T1-weighted magnetic resonance imaging on portal venous phase depicts enhancement of the septa (arrow).
담관내 유두모양 종양(intraductal papillary neoplasm of the bile duct)
담관내 유두모양 종양은 비교적 드문 질환으로 50–70대에 많이 발생하고 남자에서 조금 더 많이 발생한다고 알려져 있으며 췌장내 유두상점액종양(intraductal papillary mucinous neoplasm) 의 유사체로 간주된다[8]. 담도 내에 수많은 유두 모양으로 증식하는 종괴를 특징으로 하며 40% 정도에서 악성 부분을 포함하고 있다고 알려져 있다(Fig. 4) [9]. 초음파에서 내강 내에 종괴는 저음영 혹은 고음영으로 보이며 조영증강 초음파에서 동맥기에 조영증강을 확인할 수 있고 담도내 담관암과 달리 문맥기와 지연기에는 조영증강이 되지 않는다. 일부는 과량의 점액을 분비하여 심한 담관 확장을 일으키고 담관 내에서 담즙의 흐름을 방해하여 폐쇄성 황달, 담관염을 초래할 수도 있다. 또한, 췌장내 유두상점액종양과는 달리 악성 잠재력(malignant potential)을 가진 담관내 유두모양 종양의 특징은 잘 알려져 있지 않기 때문에 담관내 유두모양 종양은 발견하면 수술적 제거를 원칙으로 한다[10].
낭성 전이(cystic metastasis)
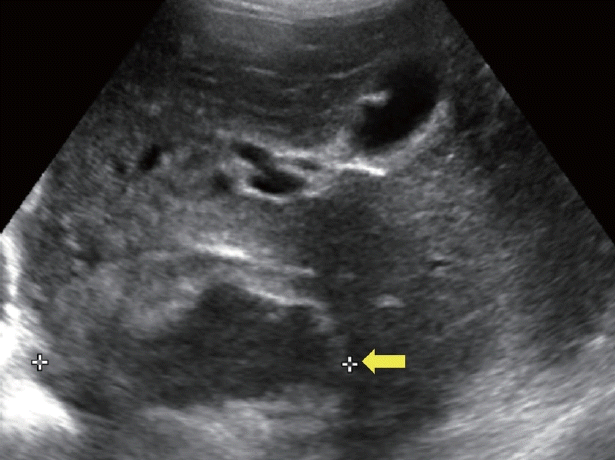
낭성 전이는 고형 전이에 비해 작게 발생하며 오로지 낭성으로만 전이되는 경우는 매우 드물다고 알려져 있다. 낭성으로 전이된 부분은 종양의 빠른 성장 속도로 인한 중심부 괴사에 의한 것이다[7]. 주로 대장, 신장, 전립선, 난소, 고환, 폐의 편평상피 세포암, 위장관 기질 종양, 육종, 신경내분비종양 등이 낭성 전이를 일으킬 수 있다. 초음파 상 낭성 전이는 단낭성 또는 다낭성일 수 있으며 두꺼운 벽을 가지고 있고 불규칙적인 모양과 벽결절(mural nodule)을 보인다(Fig. 5). 조영증강 초음파를 통해 낭종 주위의 동맥기 증강이 보일 수 있다. 하지만 진단에 초음파의 역할은 제한적이며 원발 종양에 대한 조사가 진단에 필수적이다. 낭성 전이의 치료는 원발 암의 종류, 전이의 위치 및 크기, 환자의 전반적인 건강 상태 등에 따라 달라진다.
기타 낭성 간 질환(Other cystic lesions)
담도과오종(bile duct hamartoma)
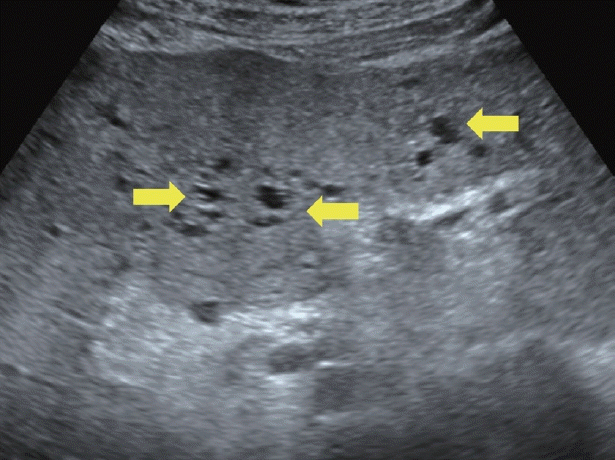
담낭과오종은 von Meyenburg complex라고도 하며 태아 발생 단계에서 작은 소엽사이담관들이 소멸되지 못하여 발생하는 양성 질환으로 부검으로 시행한 연구에서 유병률은 성인에서 5.6%로 알려져 있다[11]. 담낭과오종은 담관과는 연결되어 있지 않으며 주로 간표면 아래에 위치하거나 문맥역 주변부에 주로 위치한다. 초음파 상 1.5 cm 미만의 다발성 낭종으로 작은 크기와 낭종을 둘러싼 섬유 간질로 인해 고에코로 보일 수 있다(Fig. 6). 담낭 과오종은 T2 강조영상이 포함된 MRI와 MRCP를 통해 확진해야 한다[4]. 무증상으로 대부분 검진에서 우연히 발견되며 악성으로의 진행은 드물다고 알려져 있어 치료는 필요하지 않다. 하지만 기저 간질환이 동반되어 있는 경우 악성으로의 진행도 보고되기 때문에 추적 관찰은 기저 간질환에 준해서 시행한다[3].
담관주위낭종(peribiliary cyst)
담관주위낭종은 근외담관주위선(extramural peribiliary gland)이 염증이나 혈액 순환이상으로 인해 막힘으로써 발생하는 작은 장액성 낭이다. 간경변증이나 상염색체 우성 다낭성 신종에서 주로 발견된다고 알려져 있으며 대부분 다발성으로 발생하나 10% 정도에서 단독으로 발생할 수도 있다[12,13]. 대부분 증상 없이 우연히 발견되며 담관 폐쇄는 거의 발생하지 않는다. 초음파 상 다발성의 작은(0.1–5.5 cm) 단순 간 낭종들이 문맥 가지를 따라 진주 모양의 물방울(string of pearls)처럼 관찰된다(Fig. 7). 담관주위낭종은 근외담관주위선이 많은 왼쪽 간엽에 많이 관찰되며 담도와 연결되지는 않으나 낭종끼리 연결될 수는 있어 담도 확장과 감별이 필요하다. MRCP나 간담도기 조영제를 사용한 MRI로 담도와 연결되지 않는 것을 확인함으로써 진단에 도움을 얻을 수 있다. 무증상의 담관주위낭종은 추적이나 치료가 필요하지 않다.
포충낭(hydatid cyst)
간 포충낭은 단방 조충(echinococcus granulosus)이나 다방 조충(echinococcus multilocularis) 유충에 의한 감염에 의해 발생한다[14]. 인수공통질환으로 사람은 종숙주인 개나 늑대의 분변에 오염된 충란에 의해 감염된다[15]. 현재 우리나라에서는 거의 소멸된 것으로 알려져 있으나 해외유입 증례는 드물게 보고되고 있다[16]. 포충증은 간을 가장 흔히 침범하지만(50–60%), 폐(10–30%), 신장, 비장, 뇌 등 인체 어느 부위도 침범 가능하다. 초음파에서는 World Health Organization (WHO) 분류 기준에 따라 단순 낭종(cystic lesions), 내부에 고운 모래와 같은 음영을 보이는 낭종(cystic echinococcosis 1, CE 1), 딸낭(daughter cyst) 격막으로 인한 벌집모양 낭종(CE 2), 딸낭에 분리된 벽이 수련의 잎처럼 보이는 징후(water lily sign)를 보이는 낭종(CE 3), 딸낭이 보이지 않고 혼합 에코가 양털 뭉치처럼 보이는 징후(ball of wool sign)를 보이는 낭종(CE 4), 벽이 석회화되어 아치 모양으로 두꺼워진 낭종(CE 5)으로 보인다(Fig. 8) [14,17,18]. 초음파는 포충낭 진단의 첫 번째 영상학적 방법으로 특이도가 90%로 알려져 있으나 석회화된 벽, 딸낭, 낭종의 부피와 밀도 등을 확인하고 분류하기 위해서는 민감도와 특이도가 매우 높은 CT와 MRI를 추가로 시행해야 한다. 대부분 무증상인 경우가 많지만 우상복부 불편감, 담관염, 낭종 파열 및 아나필락시스까지 일으킬 수 있다. 치료는 WHO 분류 기준의 활동기, 과도기, 비활동기에 따라 알벤다졸과 메벤다졸과 같은 약물 치료, 수술적 제거, 경피적으로 PAIR (puncture, aspiration, injection, re-aspiration) 치료를 시행할 수 있다.

Hydatid cyst. (A) Ultrasonography of a cystic lesion with a thick, fully calcified wall (arrow). (B) Computed tomography of two peripherally calcified cystic lesions in the right hemiliver without distinct contrast enhancement (arrows). (C) World Health Organization Informal Working Group on Echinococcosis standardized classification of echinococcal cysts. Modified from the article of World Health Organization (https://www.who.int/ publications/i/item/WHO-CDS-CSR-APH-2001.6) [17]. CE, cystic echinococcosis; CL, cystic lesions.
결 론
간내 낭성 병변의 복부 초음파 진단은 비침습적이며, 빠르고 간단하게 시행할 수 있는 효과적인 검사로 일차적인 낭성 병변의 진단에 있어서 매우 유용하다. 위에서 설명한 여러 다양한 초음파적 소견을 통해 간내 낭성 병변을 분류하는데 도움을 얻을 수는 있으나 단순 간 낭종을 제외한 나머지 낭성 병변은 초음파만으로는 확진하기 어려워 CT나 MRI와 같은 영상 검사 혹은 조직검사 등의 추가 검사가 필요하다. 간종괴와 마찬가지로 간내 낭성 병변에서도 초음파의 목적은 질환의 감별보다는 발견에 초점을 두는 것이 바람직할 것으로 보인다.
Acknowledgements
I would like to express my sincere gratitude to Professor Junggil Park for sharing important cases and support throughout the research process.
This work was supported by the 2019 Inje University research grant.